31세의 한국인 과학자가 살아있는 세포의 단백질체를 분석하는 생명공학기술을 세계 최초로 개발하여, 단백질체 분석에 새로운 전기를 마련했다. 이 기술은 미토콘드리아 기질단백질체의 분석에 적용되어 495가지의 단백질들이 미토콘드리아 기질에 존재함을 밝히게 되었다.
* 미토콘드리아 기질단백질체: 미토콘드리아 기질은 내막으로 둘러싸인 공간으로 아미노산 합성, ATP 합성 등 생명에너지 발생을 하는 기관이며, 이곳에 존재하는 수백 가지의 단백질들을 기질단백질체라 한다.
미국 MIT 화학과 앨리스 팅(Alice Ting) 교수(연구책임자 및 교신저자)가 주도하고 이현우 박사(現 UNIST 나노생명화학공학부 교수)가 참여한 연구팀은 독창적으로 개발한 초미세공간 단백질체 맵핑(mapping)기술을 이용하여 세계 최초로 살아있는 세포의 미토콘드리아 기질단백질체를 확인한 연구 결과를 ‘사이언스 익스프레스’ 31일 자에 발표했다. 사이언스 익스프레스는 사이언스에 실리기 전에 중요 논문을 선정해 미리 소개하는 온라인 논문 속보다.
※ 공동 제1저자 / 논문명 : Hyun-Woo Rhee, Peng Zou / Proteomic Mapping of Mitochondria in Living Cells via Spatially-Restricted Enzymatic Tagging
생체 에너지를 만드는 미토콘드리아의 구조와 기능에 이상이 발생하면 비만, 심혈관질환, 지방간 그리고 심장질환 등을 초래해 당뇨병과 대사질환, 암, 노화, 퇴행성 신경질환(파킨슨병, 노인성 치매)이 나타난다. 이를 예방하기 위해 우리나라를 비롯한 세계 각국에서 미토콘드리아의 비밀을 밝히는 연구 프로젝트가 활발하게 진행되고 있다.
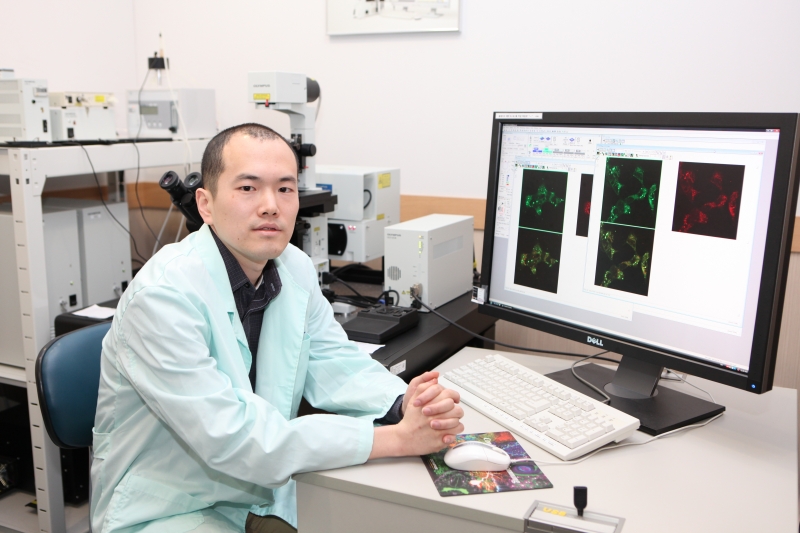
미토콘드리아 기질에서는 생명현상 유지에 필요한 아미노산의 합성이 이루어지고 생명에너지의 화폐인 ATP가 생성되지만, 미토콘드리아의 기질만을 분리해내는 기술의 부재로 아직 얼마나 다양한 단백질들이 그곳에 존재하는지 알려지지 않았다.
현재까지 미토콘드리아의 기질을 분리하기 위해서는 세포막을 벗겨 낸 죽은 세포의 세포질에서 미토콘드리아를 분리하고 이후에 미토콘드리아의 외막을 효소처리 등으로 제거한 이후에 질량분석기를 이용하여 단백질들을 분석하는 방법이 있다. 하지만 이는 다른 세포소기관 단백질들에 의한 오염 가능성이 커 꾸준히 문제가 제기되어왔다. 또한, 미토콘드리아 이외의 소포체와 같은 세포소기관도 그 분석에 어려움을 겪고 있기는 마찬가지이다.
현재의 세포소기관 연구방법은 그 과정이 번잡하고 처음에 수백 그램에서 수 킬로그램의 샘플이 필요하므로 주로 돼지, 소, 쥐 등의 장기를 토대로 연구가 진행됐다. 하지만 이렇게 밝혀진 세포소기관 단백질체조차 세포소기관 분리의 어려움으로 연구결과의 신빙성 문제가 끊임없이 제기되어왔다.
사람의 세포소기관 연구는 장기 사용에 따른 윤리적 문제로 활발한 연구가 어려웠으며, 특히 미토콘드리아와 관련된 질병의 분석에는, 현재까지 유전체(게놈) 분석에만 치중해왔을 뿐, 단백질체 분석에 기반한 연구는 활발히 이루어지지 못했다.
앨리스 팅 교수 연구팀은 살아있는 사람의 배양세포에서 특정 시간 내에 페놀라디칼을 발생시킬 수 있는 퍼옥시데이스를 이용하여서 사람의 미토콘드리아 기질단백질체를 세계최초로 규명하는 성과를 거두었다.
이번 연구결과로 세포 내 소기관 중 핵심인 미토콘드리아 내에 지금까지 알려지지 않았던 270여 개의 미토콘드리아 기질단백질을 새롭게 규명할 수 있었다. 특히 연구팀은 기존에 생물학자들이 미토콘드리아 기질 내부에 존재할 것으로 생각하지 못했던 PPOX라는 효소를 발견했다. 이번 발견은 헤모글로빈의 산소 결합 역할을 담당하는 헴(heme)의 전구물질(heme precursor)을 수송하는 단백질이 기질 내부에 있음을 의미한다. 기존의 이 효소는 미토콘드리아 이중막 사이의 공간에 있는 것으로 알려졌으나, 이번 연구로 미토콘드리아 기질에 존재함을 확인하였다.
이 연구는 기존의 수백 그램 이상의 샘플이 필요하던 방법에서 완전히 탈피하여 단 8밀리그램의 사람 배양세포의 세포질을 이용하여 이룩한 결과로써 앞으로 환자에서 얻은 미량의 조직에 포함된 미토콘드리아의 단백질체를 분석하여 진단할 수 있는 도구가 될 수 있다.
이 연구에 사용된 초미세공간의 단백질체 맵핑 기술은 미토콘드리아 기질 공간 이외의 세포의 다양한 세포소기관에 적용될 수 있는 범용적인 기술 특이성을 갖고 있으며, 따라서 세포의 다양한 세포소기관 단백질체 맵핑에 일반적으로 적용될 수 있는 매우 큰 기술파급력을 갖고 있다.
2013년 1월 1일 자로 UNIST에 임용된 이현우 교수는 “앞으로 이 논문에서 밝혀진 270여 개의 새로운 미토콘드리아 기질단백질이 미토콘드리아 생물학의 깊이를 더할 것으로 믿으며, 앞으로 본 연구에서 이용한 초미세공간 단백질체 맵핑기술이 세포소기관 단백질체 분석에 기반을 둔 질병진단의 가능성을 열 수 있다.”고 연구의의를 밝혔다.