똑같은 암을 앓는 환자라도 항암제 효능은 달라질 수 있다. 개인별 유전변이 등에 따라 항암제의 반응성이 다르게 나타나기 때문이다. 이런 환자별 결과를 미리 알려주는 인공지능(AI) 기술이 개발돼 주목받고 있다.
UNIST(총장 이용훈) 바이오메디컬공학과 이세민 교수팀은 고려대 정원기 교수팀, 한양대 서지원 교수팀과 공동으로 ‘다중 오믹스 데이터 기반의 환자 맞춤형 항암제 반응성 예측을 위한 기계학습 모델’을 개발했다. 연구진은 대규모 항암제 반응성 데이터와 다중 오믹스 데이터를 활용해 기존의 항암제 반응성 예측 모델보다 훨씬 우수한 성능을 얻었다. 네트워크 임베딩 기술과 최신 딥러닝 모델이 적용된 덕분이다.
암은 대표적인 유전체(Genome) 관련 질병, 즉 ‘게놈 병’이다. 사람마다 가진 ‘생명의 설계도’인 유전체에 계속 변이가 축적되면서 질병이 발생한다는 뜻이다. 암 조직에서는 유전자 발현 양상도 정상조직과는 달라진다. 이러한 유전변이와 유전자 발현 프로파일(Profile)은 동일 암종의 환자 간에도 상당한 차이를 보이는데, 이는 환자 특이적 항암제 반응성과 유의미한 연관성이 있다고 알려져 있다.
이에 따라, 최근에는 암 환자 특이적 유전변이나 유전자 발현 양상 등을 아우르는 다중 오믹스 데이터를 기반으로 ‘환자 맞춤형 항암제 반응성 예측 모델’을 개발하는 시도가 많다. 그러나 이런 모델 학습을 위한 생물학 데이터는 종류와 인자가 많은 데 비해 샘플 수는 부족해 기계학습 모델의 정확도를 높이는 데 한계가 있다.
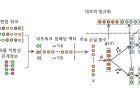
연구진은 이를 극복하기 위해 ‘네트워크 임베딩 기술’을 적용해 다차원 데이터 간의 상관관계를 효과적으로 반영했다. 먼저 암세포에서 파생된 세포주와 항암제, 유전자를 ‘노드(node, 연결점)’로 삼았다. 다음으로 각 노드를 연결해 엣지(edge, 연결선)를 만들었다. 엣지를 통해서는 항암제 반응성(세포주-항암제)이나 유전자 변이(세포주-유전자), 단백질 상호작용(유전자-유전자)에 대한 정보를 얻을 수 있다.노드와 엣지로 형성된 네트워크 세트의 상관관계를 반영한 ‘임베딩 벡터’의 추출이 이번 연구의 핵심이다. 임베딩 벡터를 이용하면 각 노드의 대푯값을 알 수 있어 고차원적인 데이터도 효과적으로 다룰 수 있기 때문이다. 연구진은 임베딩 벡터를 AI 기법인 심층신경망으로 학습시켜 환자맞춤형으로 항암제 효능을 도출했다.
제1저자인 고려대 이강근 박사는 “저항성 위주로 편향된 반응성 데이터를 보완하기 위한 다양한 인공지능 기법을 적용했다”며 “새 모델의 항암제 반응성 예측 성능은 기존 모델보다 크게 향상된 93% 정도의 정확도로 나타났다”고 설명했다.
공동 제1저자인 한양대 조동빈 연구원은 “고차원 다중 오믹스 데이터에 존재하는 요소끼리 상호작용을 효과적으로 추출하는 네트워크 임베딩 기술을 비롯한 심층신경망 등을 통해 우수한 성능을 달성했다”고 전했다.
또 다른 공동 제1저자인 UNIST 장진호 박사는 “이 기술은 암 환자에게 적합한 약물의 후보를 제안함으로써 맞춤 치료 가속화할 것”이라고 기대했다.
이번 연구결과는 생명정보학 분야 최고 학술지인 ‘브리핑스 인 바이오인포메틱스(Briefings in Bioinformatics)’에 공개됐으며, 한국연구재단의 ‘차세대정보컴퓨팅기술개발사업’과 ‘대학중점연구소지원사업’에서 지원했다.


![[연구그림] 환자맞춤형 항암제 효능 예측 모델인 RAMP의 개념도](https://news.unist.ac.kr/kor/wp-content/uploads/2022/12/연구그림-환자맞춤형-항암제-효능-예측-모델인-RAMP의-개념도-1024x310.png)