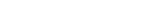UNIST(총장 이용훈) 생명과학과 박찬영 교수팀은 최근 암세포의 새로운 세포사멸 조절 기작을 발견해 암 발생에 대한 이해를 높일 수 있는 새로운 단서를 제공해 주목받고 있다.
정상적인 세포는 영양분 부족, 저산소증 등과 같은 스트레스 상황에서 세포자살(apoptosis)을 통해 사멸된다. 하지만 암세포는 스트레스 상황에서도 세포자살을 극복하고 끊임없이 증식해 암세포 자신의 생존에 유리한 기작을 발전시켜 왔다. 이러한 기작 중 최근 비사멸 세포죽음(non-apoptotic cell death) 즉, 엔토시스(Entosis)가 보고됐다.
엔토시스는 살아있는 암세포(침입세포)가 다른 암세포(포식세포) 안으로 침입해 “세포 내 세포” 구조를 만드는 일종의 세포 포식현상이다. 암세포는 엔토시스 현상을 통해 세포죽음으로 회피할 수 있는 유리한 환경을 만든다. 예를 들어 포식세포는 침입세포로부터 영양분 및 염색체를 제공받고, 침입세포는 포식세포 내에서 은신하며 적절한 상황에서 밖으로 나오거나 포식세포 안에서 세포 분열을 하기도 한다. 이러한 엔토시스는 암세포들의 상호작용으로 인한 염색체수 이상과 같은 유전체 불안정성으로 암의 발생과 발달에 영향을 미친다. 따라서, 암세포가 암을 발생시키는 원인과 치료 방법을 연구하기 위해서는 엔토시스에 대한 이해가 필요하다.
암 발생 초기에 움직임이 자유로운 암세포들(침입·포식 암세포)은 세포 내에서 혹은 세포 사이에서 특이한 신호 기전을 일으킨다. 그 중 칼슘채널 의존형 단백질의 신호전달 또한 암세포의 신호전달과 암세포 사이의 상호작용에 매우 중요한 기전으로 알려져 있었으나, 엔토시스와의 연관성에 대한 연구가 진행되지 않았다.
연구팀은 이번 연구를 통해 세포막에 존재하는 칼슘채널 단백질인 Orai1의 신호전달 기전이 암세포의 엔토시스 유도에 필수적이라는 사실을 밝혔다. Orai1은 침입 암세포와 포식 암세포에서 세포골격 단백질 중 하나인 셉틴(septin)에 의해 세포막의 특정 부위에만 국소적으로 이동하며 동일한 위치에 특징적인 패턴(oscillation)을 보이면서 세포 안에 일부분의 농도 변화를 유발한다는 점을 관측했다.
이러한 특이적 칼슘신호 전달 기전은 세포의 이동에 필수적인 동력 단백질인 마이오신을 인산화시켜 세포골격의 재배열을 유도하거나 세포가 움직이게 만든다. 이 결과를 통해 엔토시스가 유도되고 진행되는 기작을 규명할 수 있었다. 또한 Orai1 채널 혹은 신호전달 기전을 조절하면 엔토시스가 억제된다는 사실을 밝힘으로 엔토시스에 의존하는 암 발생의 조절 가능성을 제시할 수 있게 됐다.
박찬영 생명과학과 교수는 “본연구는 암발생, 전이 및 암세포의 엔토시스(세포내 세포 현상) 유발기작에 대한 오라이 칼슘채널의 새로운 신호전달기전을 구명하였다. 향후 칼슘채널 신호전달 조절 및 엔토시스 조절연구를 통해 암발생, 전이 및 치료 전략 연구에 도움이 될 것으로 기대한다.”고 전했다.
이번 연구는 과학기술정보통신부-한국연구재단의 글로벌 박사 펠로우십 사업과 중견연구자 지원사업, 선도연구센터에서 지원했으며, 연구 결과는 국제학술지 ‘Advanced Science’에 3월 24일 자로 온라인 게재됐고, 5월 17일에 출판됐다.