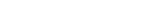단백질의 돌연변이가 백혈병 발병에 어떤 영향을 미치는지 밝혀졌다.
UNIST(총장 이용훈) 생명과학과 김홍태, 이자일 교수팀은 가톨릭대학교 김유진, 김명신 교수팀과 공동으로 혈액암의 일종인 골수형성이상증후군(Myelodysplastic syndrome, MDS)에서 돌연변이화 된 DDX41 단백질의 역할을 밝혔다. 이를 통해 유전자의 총량인 유전체의 불안정성 증가와 백혈병 발병의 연관성을 규명했다.
골수형성이상증후군은 조혈모줄기세포에서 정상 혈액세포 생성이 억제돼 말초 혈액부터 정상 혈액세포의 수가 감소하는 질환이다. 만성화되면 급성골수성백혈병(Acute myeloid leukemia, AML)으로 진행될 수 있다.
급성골수성백혈병 환자는 여성보다 남성 환자 수가 1.7배 높고, 평균 연령이 65세 이상이다. 하지만 고령화가 진행되는 지금까지도 발병 원인이 정확히 밝혀지지 않았다.
연구팀은 우리나라 336명의 골수형성이상증후군 환자의 검체에서 DDX41 유전체의 변이를 분석했다. DDX41 돌연변이인 Y259C가 골수형성이상증후군의 예후 악화와 관련이 있음을 확인했다.
특히, Y259C가 선천적으로 발생하는 돌연변이이며, 동아시아 중 한국과 일본에서 발생하는 특이적 변이임을 확인했다. 전 세계적으로 많이 나타나는 후천적 변이인 R525H와는 다르게 Y259C의 작용 원리에 대해선 알려진 바가 없었다.
DDX41은 본래 손상된 유전자를 복구시키는 단백질과 상호작용 한다. DDX41 단백질에 돌연변이가 생기면 손상된 DNA에 RNA가 붙는 고리 모양의 R-loop 구조에 의해 유전체의 불안정성이 증가된다.
R-loop의 RNA 가닥에는 m6A(n6-메틸아데노신)라는 변형 생긴다. m6A는 불안정한 R-loop의 안정성을 증가시키면서 유전체의 불안정성을 제어한다. 손상된 DNA가 복구되면 m6A가 형성된 R-loop가 해체되며 정상적인 역할을 수행한다.
연구팀은 DDX41 돌연변이를 가진 환자 검체에서 ‘m6A가 형성된 R-loop’의 발생 정도를 조사했다. 정상인 대조군에 비해 m6A가 형성된 R-loop의 양이 약 1만 배 이상 높았다. 즉, 손상된 DNA가 제대로 복구되지 않아 DNA 손상이 축적된 것이다.
더 나아가 연구팀은 DDX41 돌연변이가 m6A가 형성된 R-loop의 조절에 어떠한 영향을 미치고 어떻게 백혈병을 유발하는지 확인했다.
R-loop는 ‘메틸3’과 ‘메틸14’라는 m6A 복합체에 의해 m6A가 형성된다. ‘YTHDC1’ 단백질은 형성된 m6A를 인지하고 DNA 손상복구 단백질을 모집한다. 정상적인 DDX41은 m6A 복합체인 메틸3 또는 메틸14와 YTHDC1 단백질을 연결해주는 징검다리 역할을 한다.
하지만 DDX41 돌연변이는 징검다리 역할을 수행하지 못하게끔 막는다. 결국 DNA 손상을 복구하는 단백질의 모집이 억제돼 유전자 불안정성이 증가하고 백혈병이 발병할 수 있게 되는 것이다.
김홍태 생명과학과 교수는 “이번 연구를 통해 혈액암에서 자주 발견되는 유전적 변이인 DDX41의 분자적 역할이 세밀하게 밝혀졌다”며 “백혈병 제어 전략의 기초를 제공한 것”이라고 말했다.
이번 연구는 과학기술정보통신부 한국연구재단, 삼성미래기술육성재단의 지원을 받아 이뤄졌으며, 연구 결과는 세계적 권위의 국제학술지인 Leukemia에 3월 21일 온라인 게재됐다.