안전하면서도 비용과 시간을 줄이는 치료제 개발 전략
사스코로나바이러스-2가 전 세계에 퍼지기 시작한지도 1년이 넘었다. 한국에서만 누적 확진자가 8만 1천명을 넘었으며, 사망자도 1500명에 육박하고 있다. 초기 지역적 감염의 성공적 통제로 확산을 막는 듯했으나, 겨울이 되며 바이러스는 서울을 중심으로 빠르게 재확산됐다. 마스크가 일상화됐고, 대면 접촉을 통한 사회생활이 어려워졌다. 그래도 백신 개발에 성공하여 면역체계를 이용한 바이러스 극복 가능성을 높인 것은 반가운 소식이다.
하지만 백신과 더불어 치료제 개발도 필요하다. 앞서 바이러스를 극복한 환자에게서 얻은 혈청에서 분리한 혈청치료제, 미국 길리어드 사이언스가 개발한 렘데시비르(Remdesivir, 에볼라 바이러스의 항바이러스제로 개발됐다)가 사용된 바 있다. 그러나 임상 효과가 탁월하지는 않았다. 말라리아 치료제인 클로로퀸도 이와 비슷한 경우다. 클로로퀸은 특히 도널드 트럼프 전 미국 대통령의 언급으로 많은 관심을 받았다. 그러나 그 효과는 극히 미비한 것으로 알려졌고, 부작용도 심각해 치료제 개발의 가능성은 거의 사라졌다. 인플루엔자 바이러스의 치료제인 타미플루(Tamiflu)와 같은 코로나19에 잘 듣는 치료제의 개발이 여러 방면에서 진행 중이다.
약물 재지정을 통한 코로나19 신약 후보물질 창출
렘데시비르, 클로로퀸의 사례는 미국 식품의약국(FDA)이 승인한 기존 화합물을 코로나19 치료에 활용하려는 시도라고 할 수 있다. 이러한 신약 재창출(Drug repositioning) 방식을 ‘약물 재지정(Drug repurposing)’이라고 한다. 기존 의약품 또는 개발 후 임상 효과가 부족하여 실패한 화합물들을 다른 용도로 사용 가능한지 알아보는 방식이다.
약물 재지정 방식은 치료제 개발 비용과 시간을 현저히 줄일 수 있다는 장점이 있다. 이미 FDA의 안전성 기준 부합 여부가 검증되었기 때문이다. 즉 새로운 질병에서의 효능만 검증하면 된다. 그래서 다수의 기업 및 연구소들이 관련 연구를 활발하게 진행하고 있다.
최근 미국 샌디에고샌포드번함연구소, 중국 홍콩대, 오스트리아 비엔나대 등 국제 공동연구진은 흥미로운 결과를 발표했다. ReFRAME(Repurposing, Focused Rescue And Accelerated Medchem) 라이브러리에 등록된 1만2000개의 화합물 중 코로나19 치료제로 가능성이 있는 물질을 스크리닝한 것이다(Nature(2020) 586:113). ReFRAME 라이브러리는 FDA 등 각국의 식품의약국에 등록되거나, 임상 혹은 전임상 연구가 진행 중인 화합물들 목록이다.
이후 연구진은 코로나19 감염이 가능한 아프리카 녹색원숭이의 콩팥에서 유래된 세포(Vero E6)에 후보 화합물을 처리한 뒤, 사스코로나바이러스-2를 다시 주입하여 감염이 저해되는 약물을 선별했다. 효능을 보이는 화합물들에 대해서는 인간 세포에서도 다시 검증을 진행했다.
그 결과, 코로나19 감염 저해 효과가 있는 약 300종의 후보 화합물을 추려냈다. 레티노산수용체(retinoic acid receptor) 작용제(agnoist), 알도오스 환원효소(aldose reductase) 저해제, 벤조디아제핀수용체(benzodiazepine receptor) 작용제, 말라리아 치료제, 항염증제 등이다. 앞서 언급한 클로로퀸도 동물 및 인간 세포실험 수준에서는 효과가 있는 것으로 나타났다.
바이러스 감염 저해하는 화합물 ‘아필리모드’ 재조명
아필리모드(apillimod)는 그중에서도 눈길을 끈다. 이는 백혈구 등에서 염증을 유발하는 사이토카인(면역세포 사이 신호를 전달하는 물질)인 인터류킨-12, 인터류킨-23의 발현을 저해하는 화합물로 처음 발견됐다(Blood(2007) 109:1156). 항염증 효과가 있어 크론병, 류마티스 관절염, 건선 자가면역증 등 각종 염증유발 질병의 치료제로 임상 시험에 들어갔다. 이에 대해서는 눈에 띄는 효능이 없다는 임상 2상 결과가 나왔다.
그러나 후속 연구에서 아필리모드가 바이러스의 감염을 돕는 효소 PIKfyve의 활동을 억제한다는 것이 밝혀졌다(Chemistry & Biology(2013) 20:912). PIKfyve는 인지질의 일종인 포스파티딜 이노시톨(phosphatidyl inositol)을 변형(인산화)시키는 효소다. 인산화란 단백질을 포함한 다양한 유기 화합물에 인산기를 추가하는 화학반응을 말한다. 포스파티딜 이노시톨은 육각형 탄소화합물인 이노시톨에 사이티딘 이-인산 다이아실글라이세폴 (cytidine diphosphate diacylglycerol)이 붙은 구조다. 이는 인산화가 가능한 5부분을 가지고 있다(그림1).
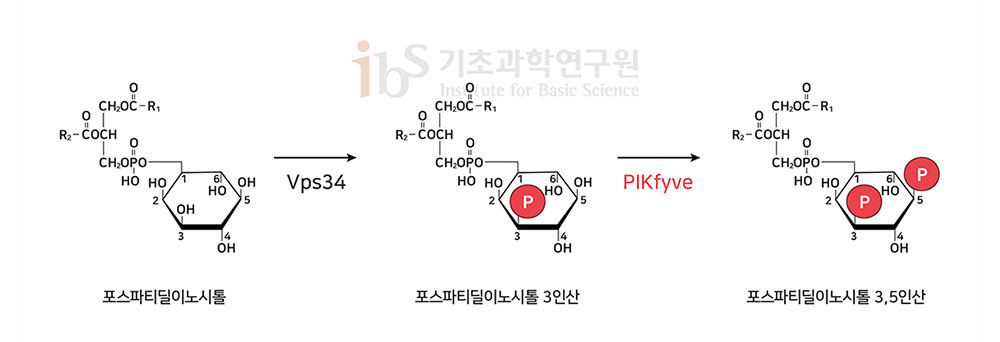
▲ 그림1. 포스파티딜 이노시톨의 인산화 과정. PIKfyve는 포스파티딜 이노시톨 3인산(PI3P)의 5번째 위치에 있는 수산기(OH)에 인산을 붙여 포스파티딜 이노시톨 3,5인산(PI(3,5)P2)을 만든다.
여러 효소들이 포스파티딜 이노시톨에 붙어있는 수산기(hydroxyl, -OH)에 인산을 붙여 세포 내 신호전달을 가능하게 한다. 포스파티딜 이노시톨은 호르몬, 신경전달물질, 성장조절인자, 삼투압 등 각종 세포 내외의 자극들에 반응하여 순차적으로 인산화가 되며 세포 내의 여러 작용 기작을 조절한다. 그중 잘 알려진 것은 세포 내 칼슘 농도를 조절하는 작용 기작이다.
최근 인산화된 포스파티딜 이노시톨이 세포의 물질 전달 과정에 사용되는 엔도솜(endosome) 형성에 중요하다는 점이 밝혀졌다. 엔도솜은 외부 물질을 세포 내로 들일 때 사용되는 구조체로서, 형성된 후에 세포 내 다른 소기관인 리소좀(lysosome)과 결합한다. 이때 엔도솜 내로 들어온 물질은 엔도솜-리소좀 복합체에서 더욱 가공 또는 파괴된다(그림2).
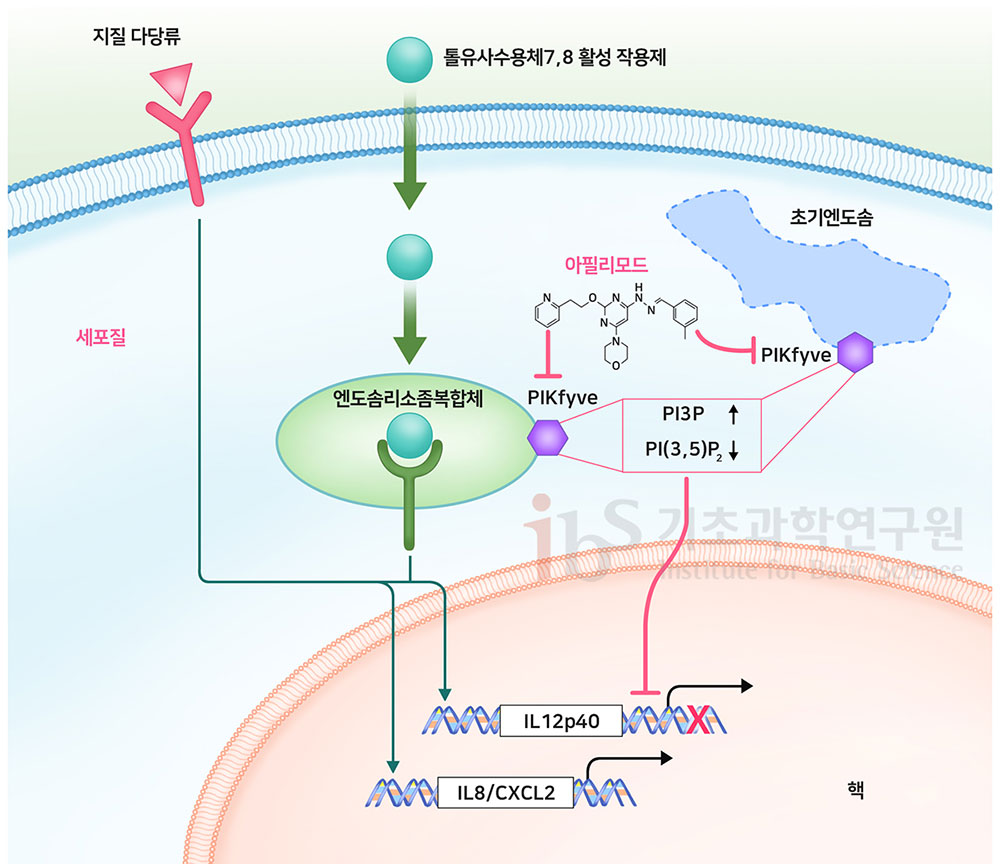
▲ 그림2. 아필리모드는 효소인 PIKfyve의 인산화 작용을 저해하여 엔도솜이 더욱 가공되는 것을 저해한다. 이로 인해 엔도솜 내에 있는 물질이 핵이나 세포내 다른 기관으로 향하는 것을 막게 된다.
가령, 포스파티딜 이노시톨(PI)의 3번째와 5번째 수산기에 인산이 붙으면, 이를 포스파티딜 이노시톨 3,5인산(PI(3,5)P2)이라 한다. PIKfyve가 포스파티딜 이노시톨을 인산화시키면(PI → PI3P → PI(3,5)P2) 엔도솜-리소좀 복합체가 형성되고 그 속에서 외부 물질이 가공된다. 요컨대 아필리모드가 효소인 PIKfyve의 활동을 억제하면, 엔도솜 내 축적된 물질이 가공되는 반응이 저해되는 것이다.
사스코로나바이러스-2, 엔도솜에 숨어 세포 감염
그렇다면 코로나19 사태에 왜 다시 아필리모드와 엔도솜이 주목받는 것일까. 바이러스가 세포를 감염시킬 때 엔도솜을 이용하기 때문이다. 바이러스의 게놈이 엔도솜에 숨어들면, 초기 면역 반응 등 숙주의 방어체제를 피할 수 있다. 사스코로나바이러스-2 역시 스파이크단백질을 이용해 ACE2 수용체에 결합한 이후, 세포의 엔도솜 기작을 이용하여 바이러스의 게놈을 세포 내로 전달한다는 것이 밝혀졌다.
사스코로나바이러스-2는 엔도솜을 이용해 숙주세포로 들어온다. 이때 아필리모드를 활용하면 엔도솜의 가공 기작을 막아 사스코로나바이러스-2 게놈의 복제를 차단할 것으로 예상된다. 실제로 미국 하버드대, 워싱턴대 등 공동연구진은 아필리모드를 활용했을 때 사스코로나바이러스-2가 더 이상 가공 또는 복제되지 않고 엔도솜 구조에 갇히는 것을 관찰했다(PNAS(2020) 117:20803). 사스코로나바이러스-2 감염을 저해할 가능성이 있다는 의미다.
포스파티딜 이노시톨의 인산화는 엔도솜 기작 조절뿐 아니라, 세포 내 칼슘 농도 조절, 특정 단백질 파괴 조절, 사이토카인 분비 억제 등에 관여한다. 따라서 아필리모드를 포함한 여러 인산화 억제제의 코로나19 치료제 개발 과정에서 부작용이 수반될 가능성이 있다. 다만 다행스럽게도 아필리모드 임상실험에서 현재까지는 큰 부작용이 발견되지 않았다.
새로운 치료제 개발에 거는 기대
약물 재지정을 통해 재조명된 화합물들은 이미 인체 내 활성과 적은 부작용 등이 검증되었다. 그래서 빠른 시간 내 치료제 개발로 이어질 수 있다는 장점이 있다. 이러한 이유에서 아필리모드와 같은 화합물로 코로나19 치료제를 개발하려는 노력도 활발히 진행 중이다. 물론 말처럼 쉬운 일은 아니다. 비유컨대 모래사장에서 바늘을 찾는 것만큼 어려운 작업이 될 것이다.
그렇다고 미리 포기할 필요는 없다. 불과 얼마 전까지만 해도, 역사상 가장 빠른 속도로 코로나19 백신을 개발할 것을 예상한 사람은 많지 않았다. 치료제 개발도 마찬가지다. 그간 축적된 기초연구의 힘으로 예상치 못했던 혁신적 결과를 낼 수 있다. 벌써 1년이 넘도록 코로나19로 인해 사회가 위축되고 많은 사람들이 고통받고 있다. 하루 빨리 좋은 치료제가 발굴되어 사회의 정상화에 기여할 수 있기를 바란다.
▣ 참고문헌
Wada, Y., Lu, R., Zhou, D., Chu, J., Pzewloka, T., Zhang, S., Li, L., Wu, Y., Qun, J., Balasubramanyam, V., et al. (2007) Selective abrogation of Th1 response by STA-5326, a potent IL-12/IL-23 inhibitor. Blood 109, 1156-1164
Cai, X., Xu, Y., Cheung, A.K., Tomlinson, R.C., Alcazar-Roman, A. Murphy, L., Billich, A., Zhang, B., et al. (2013) PIKfyve, a class III PI kinase, is the target of the small molecular IL-12/IL-23 inhibitor Apilimod and a player in Toll-like receptor signaling. Chemistry & Biology 20, 912-921
Riva, L., Yuan, S., Yin, X., Martin-Sancho, L., Matsunaga, N., Pache, L., Burgstaller-Meuhlbacher, S., De Jesus P.D., Teriete, P., Hull, M.V., et al. (2020) Discovery of SARS-Cov-2 antiviral drugs through large-scale compound repurposing. Nature 586, 113-119
Kagn, Y.-L., Chou, Y.-Y., Rothlauf, P.W., Liu, Z. Soh, T.K., Cureton, D., Case, J.B., Chen, R.E., et al., (2020) Inhibition of PIKfyve kinase prevents infection by Zaire ebolavirus and SAFS-Cov-2. Proc. Natl. Acad. Sci. U. S. A. 117, 20803-20813
글 | 명경재 기초과학연구원(IBS) 유전체 항상성 연구단 단장‧UNIST 생명과학부 특훈교수(DNA 복제·복구·재조합)
편집 | IBS 커뮤니케이션팀
발행일 | 2021년 2월 10일
※ 원문 출처 : 기초과학연구원









![[경상시론]과학자로서의 기업가](https://news.unist.ac.kr/kor/wp-content/uploads/2026/03/Entrepreneurship-190x122.jpg)
![[교수 논단] 흔들리지 않는 미래 에너지의 안정적·지속적인 확보](https://news.unist.ac.kr/kor/wp-content/uploads/2026/03/nuclear-190x122.jpg)


