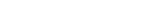‘유전자 가위’ (CRISPR) 기술로 세포 속 DNA의 움직임을 추적하는 새로운 방법이 개발됐다. 이를 통해 DNA의 응집 구조인 크로마틴 구조 변화를 실시간으로 볼 수 있다. 유전자 가위는 DNA 속 특정 영역(유전자)을 편집해 유전질환 등을 교정하는 기술이다.
UNIST (총장 이용훈) 바이오메디컬공학과 김하진 교수팀은 유전자 가위 기술을 응용해 세포 핵 속 꽁꽁 뭉쳐진 DNA의 움직임을 추적하는 기술을 개발했다. 유전자 가위는 DNA의 특정 영역(유전자)을 자르는 ‘가위 효소’와 이 효소를 안내하는 gRNA로 구성된다. 연구진은 가위 효소에 DNA의 특정 영역에 결합하는 형광 단백질을 붙여 DNA의 위치를 추적했다. 위치 추적 과정에서 ‘잡음 신호’를 줄이는 기법으로 기존의 유전자 가위 기반 이미징 방법보다 정확도와 해상도가 높을 뿐만 아니라 유전자의 위치를 장시간 추적할 수 있다. 이 덕분에 크로마틴 구조 변화를 실시간으로 관측할 수 있다.
2 m나 되는 DNA를 수 마이크론 (10-6 m) 크기의 세포핵 속에 뭉쳐놓은 구조가 크로마틴이다. 최근 크로마틴의 구조와 움직임을 파악하는 연구의 중요성이 높아지고 있다. 크로마틴 구조 이상이 암을 유발하는 것과 같은 새로운 사실이 속속들이 발견되고 있기 때문이다.
김하진 교수는 “크로마틴 구조 변화와 유전자 발현, 노화, 암 간의 정확한 연결 고리를 찾기 위해서는 크로마틴의 움직임을 실시간으로 관측하는 새로운 기술 개발이 필요하다”고 설명했다.
연구팀은 관찰하고자 하는 DNA의 특정 위치에 세 조각으로 쪼개진 형광 표지 단백질을 붙이는 방식을 썼다. 형광체에서 나오는 빛을 분석해 DNA의 위치와 모양을 알 수 있다. 형광 표지 단백질이 세 조각으로 쪼개져 있어 기존 유전자 가위 기술 기반 이미징 기법보다 원하는 부위에서만 선택적으로 신호를 얻고, 죽은 형광 신호를 되살릴 수 있다.
연구진은 DNA가 물 속 잉크가 퍼지는 것처럼 수동적인 확산을 보일 뿐만 아니라 능동적으로 위치를 옮기는 현상을 확인하였다. 새로 개발된 이미징 기법을 이용해 DNA 특정 영역의 움직임을 장시간 추적한 결과이다. 제1저자인 나렌드라 차드리 (Narendra Chaudhary) 연구원은 “DNA는 엉켜있는 긴 실과 같은 구조이기에 능동적 움직임이 없다면 부확산 (sub-diffusion)을 보일 것으로 예상됐으나, 이번 연구에서 긴 시간 동안 움직임을 측정한 결과 초확산 (super-diffusion) 현상을 보이는 것을 확인했다”고 설명했다.
이는 최근 각종 유전정보 처리 과정에서 DNA 자체가 능동적으로 움직인다는 연구결과와 일치한다. 기존에는 DNA가 움직이지 않고 단백질 효소들이 DNA를 찾아가 DNA의 고장 난 부분을 고치거나 DNA에 저장된 유전정보를 발현시키는 것으로 알려져 있었다.
김 교수는 “개발한 크로마틴 이미징 기술과 크로마틴 3차원 구조 측정 기술을 결합해 암 등의 유전체 질병에 대한 새로운 바이오마커를 발굴하고, 이를 질병의 진단과 치료에 활용할 수 있을 것”이라고 기대했다.
이번 연구는 국제학술지인 Genome Research에 9월 4일 온라인 공개됐다. 연구수행은 한국연구재단(NRF)과 기초과학연구원(IBS)의 지원을 받아 이뤄졌다.